新着情報
2023.03.01
GIPは過食・肥満・糖尿病を改善することを解明: レプチン-満腹神経系を活性化する新規インクレチン治療の確立(2023年2月28日)
2023年2月28日
GIPは過食・肥満・糖尿病を改善することを解明:
レプチン-満腹神経系を活性化する新規インクレチン治療の確立
【本研究のポイント】
・食事に伴い腸から分泌され、膵に作用してグルコース誘発インスリン分泌を促進するホルモンをインク レチンと呼び、GLP-1とGIPがある。長時間作用型のGLP-1受容体作動薬は糖尿病治療薬として使用され、血糖降下に加えて体重・摂食低下作用を示すことから、米国では肥満への適応が承認されている。
・GIPは肥満との関連が指摘されてきたにも関わらず、GIP受容体作動薬は単独およびGLP-1受容体作動薬との併用で体重・摂食低下を示すためGLP-1パラドックスとして注目されている。その解決には、GIPの体重、摂食への作用の解明が不可欠であるため、本研究では特異的なGIP受容体作動薬であるGIPFA-085の作用を調べた。
・高脂肪食負荷肥満(DIO)マウスにおいて、GIPFA-085の皮下投与は、満腹誘導・代謝亢進作用を有する脂肪ホルモン:レプチンの分泌を誘導し、摂食量低下と脂肪利用増加を起こし、1日一回連日投与することで体重および血糖値を12日目まで低下させた。一方、機能的レプチン欠損ob/obマウスではGIPFA-085は効果がなかった。
・GIPFA-085は摂食・代謝の司令塔である視床下部弓状核 proopiomelanocortin(POMC)神経を直接活性化し、その際レプチンと協働作用を発揮した。
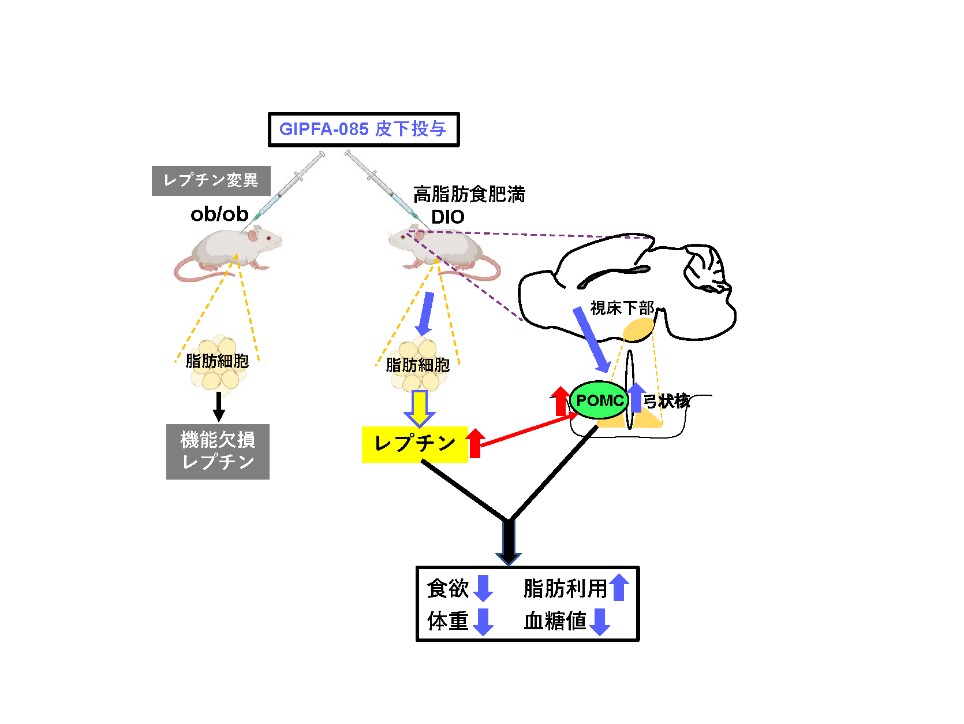
・本研究結果によって、GIPFA-085はレプチン分泌を引き起こし、レプチンとの協働作用により弓状核POMC神経を活性化させ、摂食抑制と体重低下を起こし、血糖を制御して、過食・肥満・糖尿病を改善することを明らかにした。
・本研究の意義として、(1)GIPの食欲抑制、肥満改善作用を明らかにし、(2)GIP受容体作動薬による新規インクレチン治療を確立し、(3)近く肥満を適応として承認が予想されるGIP/GLP-1二重受容体作動薬の治療の根拠を与える。
本研究成果の概要図
【研究概要】
関西電力医学研究所統合生理学研究センターおよび岐阜大学医学系研究科糖尿病・内分泌代謝内科学/膠原病・免疫内科学の矢田俊彦センター長・客員教授、韓婉昕医学研究員、矢部大介教授、関西電力医学研究所の清野裕研究所長、京都府立大学大学院生命環境科学研究科 応用生命科学専攻 岩﨑有作教授らの研究グループは、マウスを用いた研究で、インクレチンGIPの受容体作動薬がレプチン分泌を引き起こし、弓状核神経・POMC神経を活性化し、摂食抑制と脂肪利用亢進を介して体重を低下させ、血糖を制御し、食事性肥満・糖尿病を改善することを発見しました。
食事に伴い消化管から分泌され、膵に作用してグルコース誘発インスリン分泌を促進するホルモンをインクレチンと呼び、グルカゴン様ペプチド1(Glucagon-like peptide-1; GLP-1)とグルコース依存性インスリン分泌刺激ポリペプチド(Glucose-dependent insulinotropic polypeptide; GIP)があります。これらは、生体の分解酵素で速やかに切断されるため、分解酵素耐性の分子修飾をした長時間作用型の受容体作動薬が作られています。GLP-1受容体作動薬は糖尿病治療薬として広く用いられ、血糖降下に加えて体重・摂食低下作用を示し、米国では肥満への適用が承認されています。一方、GIPと肥満の関連が指摘されてきたにも関わらず、GIP受容体作動薬は単独およびGLP-1受容体作動薬との併用で体重・摂食低下を示すため、GLP-1パラドックスとして注目されています。
GIPパラドックスの解決には、GIPの体重、摂食への効果と作用機序の解明が不可欠です。本研究は、安定(半減期>6時間)で特異的なGIP受容体作動薬であるGIPFA-085を肥満・糖尿病マウスに皮下投与し作用を調べました。摂食・代謝の司令塔である視床下部弓状核神経細胞に対するGIPFA-085の作用を、Ca2+イメージングにより測定しました。
高脂肪食負荷肥満(DIO)マウスにおいて、GIPFA-085皮下投与は、投与1時間後から糖負荷試験での血糖値と摂食量(図1b)を低下させ、血中レプチン濃度を増加させました。GIPFA-085(300 nm/kg)を連日投与すると、投与後1-3日目で摂食量が低下、呼吸商が低下(脂肪利用亢進)し、1-12日目で血糖値が低下、3-12日目で体重が低下(4%)し、投与中止後リバウンドは見られませんでした。一方、機能的レプチン欠損ob/obマウスではGIPFA-085は効果を示しませんでした。GIPFA-085は弓状核のproopiomelanocortin(POMC)神経を含む満腹系神経を直接活性化し、その際レプチンと協働作用を発揮しました。
本研究結果によって、GIPFA-085はレプチン分泌を引き起こし、レプチンとの協働作用により弓状核満腹神経、POMC神経を活性化させ、摂食抑制、脂肪利用亢進、体重低下を起こし、血糖を制御して、過食・肥満・糖尿病を改善することを明らかにしました。
本研究グループは長年、インクレチンの研究を国内外で先導してきましたが、今回新たに、
(1)GIPの食欲抑制、肥満改善作用を明らかにし、
(2)GIP受容体作動薬による新規インクレチン治療を確立し、
(3)GIP受容体作動薬の治療効果に、レプチン系の状態(分泌能、抵抗性)が影響することを明らかにしました。
本研究成果は、日本時間2023年2月28日(火)20時にDiabetes Obesity And Metabolism誌のオンライン版で発表されました。
▶プレスリリースはこちら → GIPは過食・肥満・糖尿病を改善することを解明:レプチン-満腹神経系を活性化する新規インクレチン治療の確立
【問い合わせ先】
関西電力医学研究所 統合生理学研究センター センター長
矢田俊彦
電話:058-230-6372
E-mail:toshihiko.yada@kepmri.org
新着情報一覧